L’ipoadrenocorticismo o morbo di Addison è una sindrome conseguente ad una insufficiente produzione di ormoni glucocorticoidi e/o mineralcorticoidi da parte delle ghiandole surrenali. Queste due categorie di ormoni sono indispensabili per l’organismo.

Le ghiandole surrenali si compongono di una porzione più interna, detta midollare, che secerne catecolamine e di una porzione più esterna, detta corticale. Quest’ultima è a sua volta suddivisa, da un punto di vista istopatologico, in tre strati che procedendo dall’esterno verso l’interno sono: la zona glomerulosa responsabile della produzione di mineralcorticoidi (aldosterone), la zona fascicolata deputata alla sintesi di glucocorticoidi (cortisolo) e la zona reticolare nella quale vengono prodotti androgeni (Figura 2).
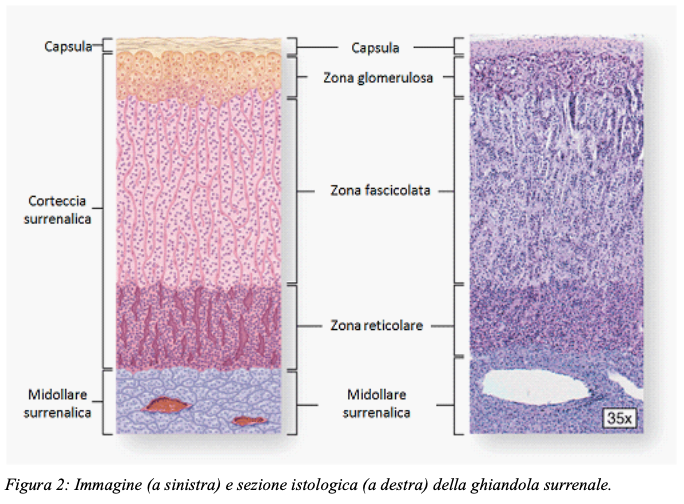
I glucocorticoidi svolgono un ruolo di vitale importanza nel mantenere una normale omeostasi. Oltre a contrastare gli effetti dello stress, il cortisolo esalta gli effetti delle catecolamine sui vasi, mantiene una normale pressione sanguigna, stimola la gluconeogenesi epatica e il catabolismo di proteine e grassi, garantisce una corretta funzionalità e integrità della mucosa gastrointestinale.
La carenza di questo ormone comporta quindi una maggiore sensibilità allo stress, l’incapacità di mantenere il tono vasale, l’integrità endoteliale e la conseguente ipotensione, ipoglicemia e debolezza muscolare, sintomi gastroenterici quali disoressia/anoressia, vomito e diarrea.
La sintesi e secrezione di aldosterone, principale rappresentante dei mineralcorticoidi, è regolata dall’asse renina-angiotensina, dalla concentrazione plasmatica di potassio e, per una quota quasi trascurabile, dalla concentrazione di ACTH.
Aumentando l’assorbimento di sodio (e indirettamente di acqua) e la secrezione di potassio e ioni idrogeno a livello renale e in altri siti meno rilevanti, l’aldosterone svolge un ruolo fondamentale nel garantire l’equilibrio salino dell’organismo e ne condiziona in parte anche il pH.
Pertanto, una carenza di tale ormone comporta lo svilupparsi di alterazioni elettrolitiche (iponatremia, ipocloremia, iperkaliemia e acidosi metabolica). Le perdite idriche conseguenti alla mancata capacità di trattenere sodio e cloro comportano una riduzione del fluido extracellulare che, nel tempo, esitano inevitabilmente in una condizione di ipovolemia, ipotensione, riduzione della gittata cardiaca, riduzione della filtrazione glomerulare e iperazotemia prerenale.
Classificazione:
L’ipoadrenocorticismo primario, più frequente (circa il 95% dei casi), è causato da una distruzione di entrambe le ghiandole surrenali conseguente, quasi sempre, ad un meccanismo autoimmune, e si rende clinicamente manifesta solo quando è interessato più del 90% della corteccia surrenalica.
Altre possibili cause di distruzione della corteccia surrenalica, sebbene più insolite, sono alcune patologie granulomatose specifiche (quali l’istoplasmosi e la blastomicosi), l’amiloidosi, lesioni ischemiche da infarti emorragici locali (secondari a traumatismi a coagulopatie o a tossicosi da anticoagulanti cumarinici) o anche neoplasie metastatiche (carcinomi polmonari, mammari, prostatici, gastrici e pancreatici, o melanomi).
L’ipocortisolismo primario può infine verificarsi anche per cause iatrogene conseguenti ad eccessiva somministrazione di farmaci, quali mitotane e trilostano, utilizzati per il trattamento dell’ipercortisolismo.
Sono interessati soprattutto soggetti giovani e di mezza età con una età mediana di 4 anni (da 4 mesi a 14 anni) (Peterson et al, 1996).
L’ipoadrenocorticismo secondario, invece, è causato da una ridotta secrezione dell’ormone trofico specifico (ormone adrenocorticotropo o ACTH) da parte dell’ipofisi.
Nel cane, come nell’uomo, questa condizione è generalmente conseguente a processi neoplastici, meno comunemente a problemi infiammatori o traumatici.
Il mancato stimolo da parte dell’ACTH determina l’atrofia della zona fascicolata e, conseguentemente, una carenza glucocorticoidea.
Il trattamento protratto con farmaci corticosteroidi inibisce l’asse ipotalamo-ipofisario e può quindi comportare atrofia surrenalica secondaria.
La sensibilità individuale ai corticosteroidi è molto variabile: in alcuni individui l’atrofia della corticale si instaura dopo pochi giorni di somministrazione, in altri individui questo non accade. La soppressione dell’asse ipotalamo-ipofisario-corticosurrenalico può persistere per settimane o mesi dopo la sospensione dei glucocorticoidi, a seconda della dose, della preparazione, della durata del trattamento e della sensibilità individuale.
Solitamente l’insufficienza surrenalica iatrogena si verifica in seguito a terapie croniche; è stata documentata non solo con glucocorticoidi iniettabili od orali, ma anche con farmaci ad uso topico dermatologico, oftalmico ed auricolare. Pertanto, l’effettuazione di test di funzionalità surrenalica in soggetti sottoposti a terapie corticosteroidee deve essere posticipata da un minimo di 48 ore (nel caso di una singola somministrazione di prednisone o prednisolone) fino a 6-8 settimane dalla sospensione del farmaco (nel caso di forme deposito) per poter garantire una interpretazione corretta dei risultati .
Per questo motivo la forma secondaria è caratterizzata dalla sola carenza glucocorticoidea, mentre la forma primaria si associa generalmente a carenza sia glucocorticoidea che mineralcorticoidea.
Tuttavia, oltre un 30% dei casi di ipoadrenocorticismo primario presenta, al momento della diagnosi, concentrazioni elettrolitiche normali; tali casi potrebbero essere confusi con forme secondarie. Questa condizione, più insidiosa da diagnosticare, è stata definita “atipica”.
La discriminante in questo caso è rappresentata dalla concentrazione di ACTH endogeno che risulta bassa nel caso della forma secondaria, mentre è elevata nella forma primaria. Possibili ipotesi che giustifichino l’assenza di alterazioni elettrolitiche sono: un coinvolgimento più tardivo della zona glomerulosa, l’influenza di malattie concomitanti (es. ipotiroidismo) oppure altri fattori, diversi dall’aldosterone, implicati nel mantenere l’equilibrio elettrolitico.
Nel cane l’ipoadrenocorticismo è una patologia piuttosto rara, un recente studio del 2016 ha individuato una incidenza di 2,3 casi ogni 10000 soggetti.
Ad eccezione di queste razze, per le quali non è stata dimostrata una predisposizione di sesso, nella popolazione generale è stata individuata una predisposizione per il sesso femminile (circa del 70%) e una probabilità 3 volte maggiore per i soggetti sterilizzati (sia maschi che femmine) rispetto ai soggetti interi di contrarre la malattia.
Sintomatologia:
I segni clinici in corso di Ipoadrenocorticismo ipofisario o Morbo di Addison canino possono comparire in maniera acuta o stabilirsi in modo graduale, in quest’ultimo caso caratterizzati da un andamento “altalenante” (sintomi che “vanno e vengono”), e la cosiddetta crisi addisoniana è in genere scatenata da un evento stressante.
|
Preoccupazione dei proprietari |
Peterson e coll. (1996) |
Feldman e Nelson (2004) |
|
Anoressia |
91,6% |
88% |
|
Letargia |
93,8% |
85% |
|
Dimagramento |
48% |
82% |
|
Vomito |
76,4% |
68% |
|
Debolezza/astenia |
|
51% |
|
Diarrea |
41,3% |
35% |
|
Sintomi “altalenanti” |
43,1% |
25% |
|
Tremori |
27,1% |
17% |
|
Poliuria/polidipsia |
24% |
17% |
|
Collasso |
|
10% |
|
Addome dolente |
|
8% |
|
Sintomi Clinici alla visita |
Peterson e coll. (1996) |
Feldman e Nelson (2004) |
|
Letargia/depressione |
86,2% |
87% |
|
Dimagramento |
|
82% |
|
Debolezza/astenia |
76,4% |
66% |
|
Disidratazione |
46,2% |
41% |
|
Collasso |
34,7% |
24% |
|
Polso debole |
34,7% |
22% |
|
Bradicardia |
|
22% |
|
Prolungamento TRC |
34,7% |
|
|
Melena/ematochezia |
15,1% |
17% |
|
Ipotermia |
33,8% |
15% |
|
Addome dolente |
|
7% |
Per giungere alla diagnosi di questa patologia piuttosto rara, il veterinario, a seconda della presentazione del paziente e della successiva visita clinica, potrà richiedere alcuni esami sia di laboratorio che strumentali (Emogramma, Profilo biochimico, Ecografia addominale, RX toracico , Elettrocardiogramma).
Emocromocitometrico: Le alterazioni più comunemente riscontrate all’esame emocromocitometrico sono rappresentate da un lieve stato di anemia normocitica normocromica non rigenerativa e, decisamente più caratteristico, da un quadro di linfocitosi ed eosinofilia.
Profilo biochimico: Per quanto riguarda le altre alterazioni al profilo biochimico, quelle senza dubbio più frequenti sono quelle relative alla funzionalità renale. L’incremento di urea e creatinina è dovuto solitamente ad una grave insufficienza “prerenale” conseguente allo stato di ipovolemia, ipotensione e ridotta perfusione renale.
|
|
Peterson e coll. (1996) |
Melian e Peterson (1996) |
Feldman e Nelson (2004) |
|
Ipercalcemia |
30,7% |
19,1% |
29% |
|
Ipoglicemia |
16,7% |
35% |
22,9% |
|
Ipoprotidemia |
12,5% |
23,8% |
14% |
|
Ipoalbuminemia |
6,3% |
12,2% |
18% |
|
Iperazotemia |
88,4% |
76,2% |
88,5% |
|
Aumento della creatininemia |
65,6% |
59,5% |
61% |
|
PS urinario<1030 |
57,6% |
61,9% |
88% |
|
Acidosi |
|
65,9% |
50% |
|
Aumento ALT |
28,7% |
56,1% |
|
|
Aumento AST |
30,7% |
38,1% |
|
|
Aumento SAP |
31,1% |
26,8% |
|
Diagnostica per immagini: I cani colpiti da Ipoadrenocorticismo possono mostrare segni radiografici di ipovolemia. La gravità dei suddetti riscontri radiografici è solitamente correlata al grado di ipovolemia, quindi sarà maggiore nei soggetti che presentano anche insufficienza mineralcorticoidea. L'ecografia: delle ghiandole surrenali sembra rappresentare un utile mezzo diagnostico per il morbo di Addison, soprattutto come test di screening in caso di crisi surrenaliche acute.
Diagnosi e terapia: Nel caso la valutazione clinica e gli esami effettuati indirizzino verso la diagnosi di Ipoadrenocorticismo ipofisario o morbo di Addison, il veterinario potrà richiedere ulteriori esami specifici per confermare la diagnosi.





Lascia i tuoi commenti
Posta commento come visitatore